 29
29 
Некоторые спорные вопросы консервативной терапии острого панкреатита
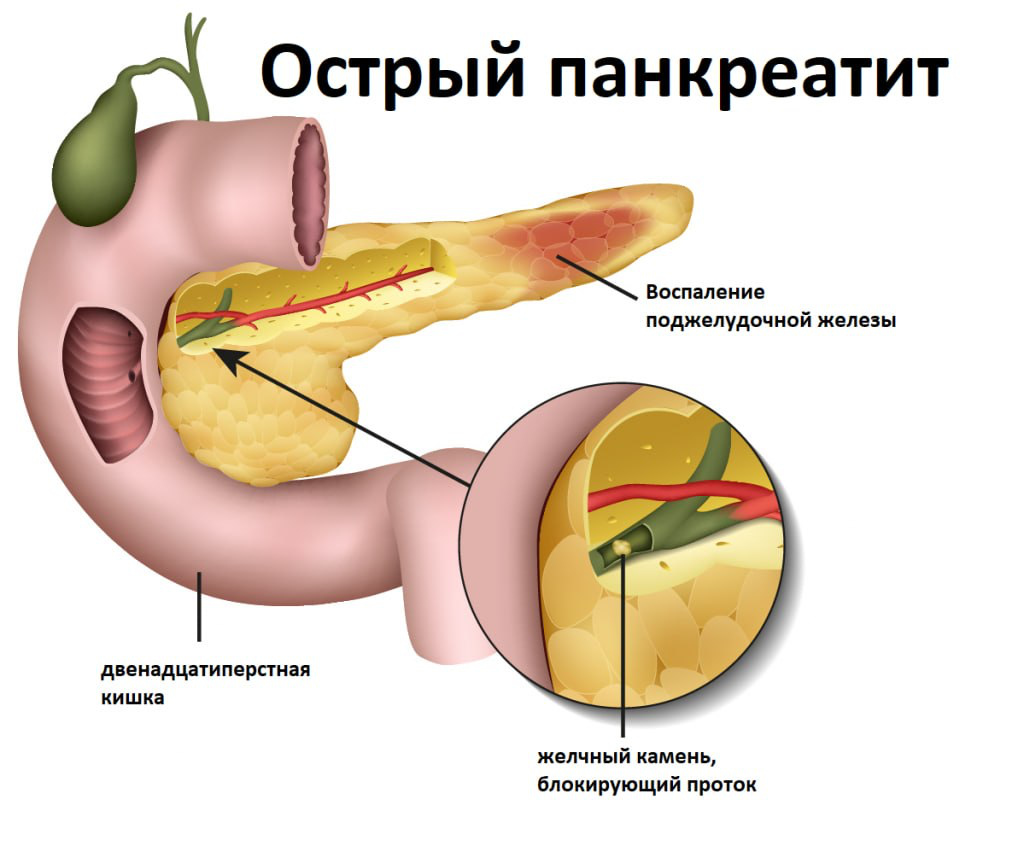
Острый панкреатит (ОП) – острое асептическое воспаление ткани поджелудочной железы демаркационного типа, в основе которого лежат острая дистрофия, ферментная аутоагрессия с некробиозом панкреатоцитов и последующим исходом в некроз ткани железы и окружающих структур с присоединением эндогенной вторичной гнойной инфекции или в склероз поджелудочной железы с атрофией ее железистого аппарата.
На сегодняшний день опубликовано очень много работ, посвященных проблеме ОП, но до сих пор большинство положений относительно этиологии, патогенеза, классификации и лечебной тактики вызывают дискуссии. Принято считать ОП полиэтиологическим заболеванием. При этом американские авторы основной его причиной считают злоупотребление алкоголем, немецкие – желчнокаменную болезнь, китайские и вьетнамские авторы – аскаридоз. Тем не менее, традиционно выделяют две группы этиологических факторов ОП.
К первой группе относятся факторы, определяющие нарушение оттока панкреатического секрета из ацинусов по внутридольковым протокам в главный панкреатический проток и далее в ДПК, что приводит к резкому повышению давления в протоковой системе поджелудочной железы (гипертензионно-протоковые факторы).
Этиологические факторы, относящиеся ко второй группе, приводят к первичному поражению ацинарных клеток в условиях нормального внутрипротокового давления (первично ацинарные факторы). Известно, что первичное поражение ацинарных клеток поджелудочной железы может возникать при локальных расстройствах гемоперфузии, аллергических реакциях, метаболических нарушениях, гормональном дисбалансе, токсических воздействиях, инфекциях, травме поджелудочной железы.
Таким образом, основными этиологическими факторами ОП можно назвать следующие: желчнокаменная болезнь, патология терминального отдела общего желчного протока и БДС, злоупотребление алкоголем, травмы (в т. ч. и операционные) поджелудочной железы, сосудистые заболевания, нарушения обмена веществ, инфекции, интоксикации, аутоаллергические состояния. Экспериментально показано и подтверждено клинически, что наиболее тяжелые формы ОП развиваются при сочетании трех этиологических факторов:
- панкреатической гиперсекреции;
- острой внутрипротоковой гипертензии;
- внутриканальцевой активации панкреатических ферментов.
Патогенез ОП в настоящее время также остается предметом острых дискуссий. Считается, что к развитию ОП приводит нарушение внутриклеточного образования и транспорта ферментов поджелудочной железы, а также интраацинарная активация проферментов гидролазами. Пусковым механизмом патологических реакций, являющихся основой воспалительно-некротического поражения поджелудочной железы, служит высвобождение из ацинарных клеток активированных панкреатических ферментов, в норме присутствующих в виде неактивных проферментов. При этом сегодня принято считать, что процессы аутолиза первично обусловлены действием именно липолитических ферментов. Активация липаз происходит при контакте проферментов последних с желчными кислотами и энтерокиназами. Данная ситуация возникает при гидравлической деструкции ацинусов вследствие внутрипротоковой гипертензии, которая является, в основном, следствием гиперсекреции поджелудочной железы и билиарно-панкреатического или дуодено-панкреатического рефлюкса при стенозе или недостаточности сфинктера Одди и дуоденальной гипертензии. Предполагается, что алкоголь оказывает не только непосредственный токсический эффект на панкреатоциты, но также вызывает образование белковых микроконгломератов, окклюзирующих мелкие панкреатические протоки. Заметим, что липаза поджелудочной железы не повреждает здоровую клетку. Повреждение обусловлено действием фосфолипазы А, приводящим к деструкции клеточных мембран, что делает возможным проникновение в клетку липазы. При реализации данного механизма формируются локусы жирового панкреонекробиоза с перифокальным демаркационным валом. Если патобиохимический процесс ограничивается этим, то формируется жировой панкреонекроз. В том случае, если при чрезмерном накоплении в ткани железы жирных кислот рН достигает 3, 4 - 4, 3, происходит трансформация внутриклеточного трипсиногена в трипсин. При этом трипсин активирует проферменты лизосом, а также другие протеиназы, вызывающие протеолиз панкреатоцитов. Активированная эластаза лизирует стенки сосудов, междольковые соединительнотканные перемычки, что способствует быстрому распространению ферментного аутолиза в поджелудочной железе и в окружающих структурах. Под действием трипсина активизируются все проферменты поджелудочной железы (эластазы, карбоксипептидазы, профермент химотрипсина), проферменты калликреин-кининовой системы, фибринолитические ферменты и профакторы гемокоагуляции, что, в конечном счете, приводит к местным и общим патобиохимическим расстройствам с возможным финалом в виде синдрома полиорганной недостаточности. Принято выделять доинфекционную стадию заболевания, при которой формируются асептические воспалительные и некротические очаги, и фазу инфекционных осложнений – инфицированный панкреонекроз, инфицированный панкреонекроз с панкреатогенным абсцессом, забрюшинная флегмона.
В настоящее время принципиальные положения консервативного лечения ОП изложены во всех руководствах по неотложной абдоминальной хирургии. Позволим напомнить их читателю с некоторыми комментариями. Итак, при ОП показаны:
- Мероприятия, направленные на угнетение экзокринной функции поджелудочной железы: А) «Холод, голод и покой» (локальная гипотермия, строгая диета, постельный режим) ; Б) Медикаментозное подавление панкреатической секреции: цитостатики (5-фторурацил, тегафур), ингибиторы желудочной секреции (антисекреторные препараты – Н2-блокаторы, ИПП), агонисты опиоидных рецепторов (даларгин), панкреатическая рибонуклеаза, соматостатин и его синтетические аналоги (октреотид).
- Спазмолитическая терапия: миотропные спазмолитики (дротаверин, папаверин), холинолитики (платифиллин, атропин), инфузии глюкозо-новокаиновой смеси.
- Мероприятия, направленные на инактивацию циркулирующих в крови панкреатических ферментов и торможение каскада реакций калликреин-кининовой системы: ингибиторы протеаз – апротинин, ε- аминокапроновая кислота.
- Купирование болевого синдрома: нестероидные противовоспалительные препараты, опиоидные (разумеется, за исключением морфина) анальгетики, регионарные новокаиновые блокады.
- Коррекция гиповолемических и водно-электролитных расстройств, улучшение микроциркуляции, ингибирование свободно-радикального окисления: инфузии кристаллоидов, коллоидов (препараты гидроксикрахмала, желатины), перфторорганические эмульсии, альбумин, свежезамороженная плазма, специфические и неспецифические антиоксиданты.
- Дезинтоксикационная терапия и методы афферентной детоксикации: инфузии декстранов, форсированный диурез, экстракорапоральная детоксикация (гемо-, лимфо- и энтеросорбция, плазмаферез, ультрагемофильтрация).
- Восполнение энергетических затрат (не менее 3500 ккал/сут): парентеральное питание, сбалансированное энтеральное зондовое питание.
- Коррекция синдрома энтеральной недостаточности: профилактика или купирование пареза кишечника, декомпрессия тонкой и толстой кишки, энтеральный лаваж, применение энтеросорбентов, антигипоксантов.
- Превентивное назначение антибактериальных препаратов: цефалоспорины III поколения, фторхинолоны, метронидазол, при развившемся панкреонекрозе – карбапенемы (меропенем).
- Посиндромная терапия.
В работах различных авторов за последние пять-десять лет отчетливо прослеживается эволюция лечебной тактики у больных с ОП от агрессивной хирургической до консервативной выжидательной. Однако единого общепринятого подхода к фармакотерапии ОП до сих пор нет.
Следует отметить, что непременным условием лечения пациентов с любой клинико-морфологической формой ОП является соблюдение главного условия – создания покоя для поджелудочной железы. Это достигается путем подавления продукции ферментов панкреатоцитами, вследствие чего значительно уменьшается выделение ферментов, лизирующих белки (трипсин, химотрипсин, эластаза) и фосфолипидные мембраны клеток (фосфолипазы, холестеролэстераза). Таким образом, состояние покоя панкреатоцита способствует регрессу аутолиза и предупреждает некротические изменения тканей. В этой связи в комплексной терапии ОП ведущее место занимают препараты, прямо или косвенно угнетающие экзокринную функцию поджелудочной железы. Максимальный лечебный эффект достигается при синергичном подавлении синтеза ферментов на уровне поджелудочной железы, выведении и инактивации уже циркулирующих в крови энзимов.
Вместе с тем, во многих аспектах консервативного лечения существуют различные мнения и подходы. В данной статье мы рассмотрим только некоторые из них.
Так, например, остаточно спорной на сегодняшний день является стратегия применения препаратов соматостатина (СС) и его аналогов. Механизм их действия в физиологических условиях многогранен, реализуется через непосредственное связывание СС с рецепторами на ацинарных клетках и подавление секреции ПЖ, а также за счет торможения синтеза секретина, холецистокинина и других гормонов желудочно-кишечного тракта. Однако массивная внутриклеточная активация предсуществующих ферментов при ОП путем обратной связи блокирует синтез новых энзимов, что является естественным механизмом угнетения секреции. Доказано, что в данной ситуации уменьшается и экспрессия рецепторов к СС на рецепторах ацинарных клеток. Наблюдаемые антивоспалительный и цитопротективный эффект СС и его полусинтетических аналогов реализуются за счет изменения обмена эйкозаноидов. Выявлено, что СС в большей степени влияет на механизмы воспаления и в меньшей - на уровень ферментемии при ОП [59]. Данные об эффективности СС при экспериментальном ОП и в клинической практике противоречивы. Авторы исследований, проведенных на лабораторных животных, считают СС и его аналоги эталонами в лечении деструктивного ОП и сравнивают с ним другие средства. Самое крупное проспективное многоцентровое рандомизированное клиническое исследование, посвященное данному вопросу, было проведено в Германии (302 пациента). По результатам работы не было выявлено достоверных отличий в отношении летальности, количества осложнений, хирургических вмешательств и длительности пребывания в стационаре в группах с применением октреотида и плацебо. Мета-анализ 4 клинических исследований показал, что октреотид не уменьшает количество хирургических вмешательств у больных с ОП, не снижает частоту развития сепсиса, не уменьшает летальность, а также общее количество осложнений, поэтому не может быть рекомендован для рутинного применения при ОП. Положительные результаты применения СС при экспериментальном ОП и неоднозначные клинические результаты могут быть объяснены следующим. В опытах на лабораторных животных исследователи использовали совершенно иную схему введения препарата (перед воздействием этиологического фактора или в первые минуты после него), а выбранные авторами дозировки лекарственного средства в десятки раз превышали применяемые в хирургической практике. Остается дискутабельным вопрос о целесообразности использования ингибиторов протеаз (ИП). Известен 50-летний опыт их применения при ОП, но большинство ранее проведенных исследований не соответствовали требованиям доказательной медицины, а в мета - анализе результаты использования ИП однозначно признаны неприемлемыми. Несмотря на противоречивость данных, ИП в настоящее время включены в протоколы лечения больных тяжелым ОП во многих странах.
Другой аспект консервативного лечения, по которому не существует единого мнения – это вопрос профилактического назначения антибиотиков при диагностированном деструктивном панкреатите, а также стратегия антибактериальной терапии при его инфицированных формах. Известно, что летальность от инфицированного панкреонекроза в 2-3 раза выше, чем при стерильном процессе. Представляется логичным включать в базисную терапию ОП антибиотики для снижения частоты инфицирования, что могло бы привести к патогенетически обоснованному снижению частоты гнойных осложнений и улучшить прогноз. Однако в рандомизированных исследованиях по профилактическому назначению антибиотиков при некротическом ОП не было обнаружено статистически значимого уменьшения частоты развития инфицированного некроза, инфекционных осложнений экстрапанкреатической локализации, неблагоприятных исходов заболевания. Также не было выявлено влияния на потребность в оперативном лечении и возникновение микозов. Из всех групп антибактериальных препаратов, применяемых в хирургии, только карбапенемы достоверно снижают частоту инфицирования панкреатического некроза, но влияние этих средств на другие указанные выше показатели статистически не значимо. В каждую из приведенных работ было включено небольшое количество пациентов (не более 114), лишь некоторые из проведенных исследований были двойными слепыми плацебо-контролируемыми. Ряд авторов рассматривают как единственное рациональное показание к назначению антибиотиков подтверждение панкреатической инфекции. В то же время, прогнозирование и диагностика инфицированного панкреонекроза представляют определенные трудности. Распространенные формы некротического ОП практически всегда инфицируются, причем в некоторых случаях уже на первой неделе заболевания. Наряду с клиническим ухудшением состояния больного (нарастание интоксикации, ПОН, стойкая лихорадка) опорными лабораторными критериями служат следующие: повышение в плазме крови уровней С-реактивного белка (СРБ) более 60-80 мг/л, прокальцитонина свыше 1,8 нг/мл, значительное увеличение концентраций ИЛ-6, ИЛ-8. Однако количественное определение указанных серологических маркеров, за исключением СРБ, не является широкодоступным. Наибольшей чувствительностью и специфичностью (до 90%) обладает тонкоигольная аспирационная биопсия под ультрасонографическим наведением или под контролем компьютерной томографии, хотя, ввиду инвазивности процедуры, она сама по себе может привести к инфицированию. В большинстве клиник России и зарубежных стран все же используется раннее назначение антибиотиков при панкреонекрозе, что связано как с трудностью своевременной и точной дифференциальной диагностики стерильных и инфицированных форм, так и с наличием многолетнего опыта, указывающего на возможность только консервативного лечения некротического панкреатита. Большую роль играет также высокий риск развития пневмонии у данной категории тяжелых больных, а также другие ситуации.
Вопросы иммунокоррекции при ОП также не имеют однозначного понимания среди хирургов и реаниматологов. Большинство специалистов признает необходимость иммунотерапии при тяжелых формах. Есть публикации, в которых даны четкие рекомендации по целенаправленному применению ронколейкина и других средств, которые способны опосредованно воздействовать на иммунокомпетентные клетки (рефортан, лонгидаза, ксефокам, глутоксим). Однако при анализе приведенных авторами результатов обращает на себя внимание полиморфизм изменений Т–клеточного звена, разнонаправленность их при определенных этиологических формах ОП, сложность трактовки указанных изменений и обоснования проводимой терапии. Существует и другое мнение, согласно которому для прогноза течения ОП имеет значение адекватная воспалительная реакция, характер которой детерминирован определенными аллелями генов, кодирующих продукцию многочисленных компонентов иммунного ответа, поэтому назначение иммунокорректоров с научной точки зрения еще предстоит разработать.
В заключение можно сказать, что консервативное лечение во многих случаях позволяет прервать каскад патологических реакций, развивающихся при тяжелых формах острого панкреатита. Эффективность проводимых мероприятий прямо зависит от четкого определения показаний, времени начала терапии, адекватности ее объема, преемственности в работе всех специалистов. Всеми панкреатологическими школами мира признана необходимость мультидисциплинарного подхода в ведении пациентов с некротическим ОП. Достигнутые на современном этапе успехи позволяют рассматривать хирургические вмешательства при данной патологии как имеющие вынужденный характер. Лечение этой категории больных подразумевает ясное понимание того, что происходит в ПЖ и организме в целом в разные фазы течения болезни и каковы механизмы лечебного воздействия. Несмотря на признание во всем мире консервативных мероприятий как первого, базового этапа лечения ОП, по многим аспектам терапии нет единого мнения. Вышеизложенное диктует необходимость продолжения фундаментальных исследований патогенеза, диагностики и лечения данного заболевания.



 info@mmd-ad.ru
info@mmd-ad.ru